|
Emmanuelle Charpentier y
Jennifer Doudna
han recibido el Premio Nobel de Química 2020 por descubrir
una de las herramientas más útiles usadas en la tecnología
genética: las tijeras genéticas o CRISPR/Cas9. Los
investigadores pueden utilizarlas para cambiar el ADN de
animales, plantas y microorganismos con una precisión
extremadamente alta. Esta tecnología ha revolucionado las
ciencias biológicas, trayendo nuevas oportunidades para el
mejoramiento de los cultivos o contribuyendo a terapias
innovadoras contra el cáncer que pueden hacer realidad el
sueño de curar enfermedades hereditarias. |
|
El editor de genes, CRISPR-Cas9, es uno de esos descubrimientos
con un potencial impresionante. Cuando Emmanuelle Charpentier y Jennifer Doudna comenzaron a
investigar el sistema inmunológico de una bacteria
Streptococcus, pensaban que tal vez podrían desarrollar
una nuevo antibiótico. En cambio descubrieron una
herramienta molecular que puede usarse para hacer cortes
muy precisos en el material genético, posibilitando
cambios en el código de la vida.
|
|
|
En 2002, cuando Emmanuelle
Charpentier fundó su propio grupo de investigación en la
Universidad de Viena, se centró en una de las bacterias
que más daño causa a la humanidad: el Streptococcus
pyogenes, que cada año infecta a millones de personas.
Para comprender mejor la bacteria S. pyogenes, Charpentier
comenzó investigando a fondo sus genes. Esta decisión fue
el primer paso en el camino hacia el descubrimiento de las
tijeras genéticas
En 2006 Jennifer Doudna
dirigía un grupo de investigación en Berkley (Universidad
de California) y ya acumulaba dos décadas de experiencia
trabajando con ARN. Estaba considerada como una
investigadora de éxito, con olfato para proyectos
innovadores, que recientemente había entrado en un campo
nuevo y emocionante: el ARN interferente.
|
|
Un colega, microbiólogo,
le comenta a Doudna su descubrimiento: cuando se
comparan el material genético de diferentes bacterias,
y también de las arqueas (un tipo de microorganismo),
se encuentran secuencias de ADN repetitivas que están
sorprendentemente bien conservadas. El mismo código
aparece una y otra vez, pero entre las repeticiones
hay secuencias que llaman la atención (ver figura 1).
Es como si, en un libro, una misma palabra se
repitiera entre las oraciones.
Estas matrices de
secuencias repetidas se denominan repeticiones
palindrómicas cortas, agrupadas y regularmente
espaciadas (clustered regularly interspaced short
palindromic repeats),
abreviadas como CRISPR. Lo interesante es
que las secuencias únicas y no repetitivas en CRISPR
(situadas tras las repeticiones) parecen coincidir con
el código genético de varios virus, por lo que el
pensamiento actual es que son parte de un
antiguo sistema inmunológico que protege a las
bacterias y arqueas de los virus. La hipótesis es que
si una bacteria ha logrado sobrevivir a una infección
por virus, agrega una parte del código genético del
virus a su genoma como un recuerdo de la infección.
También se han
descubierto genes especiales, asociados a CRISPR, que
se han denominado con la abreviatura Cas. Doudna se dio
cuenta de que estos genes son muy similares a los
genes que codifican las proteínas que desenrollan y
cortan el ADN. Entonces, ¿las proteínas Cas tienen la
misma función? ¿Cortan el ADN del virus?
Su grupo de
investigación comienza a trabajar en este problema y,
después de unos años, logran revelar la función de
varias proteínas Cas diferentes.
Paralelamente Emmanuelle Charpentier investigaba las pequeñas moléculas de
ARN que regulan los genes y, en colaboración con
investigadores de Berlín, había mapeado los pequeños
ARN que se encuentran en S. pyogenes.
Charpentier muestra que
la molécula de ARN, que denomina ARN crispr
trans-activador (ARN tracr), también tiene una
función decisiva, es necesario para que el ARN que se
crea a partir de la secuencia CRISPR en el genoma
evolucione hacia su forma activa (ver figura 1 ). |
|
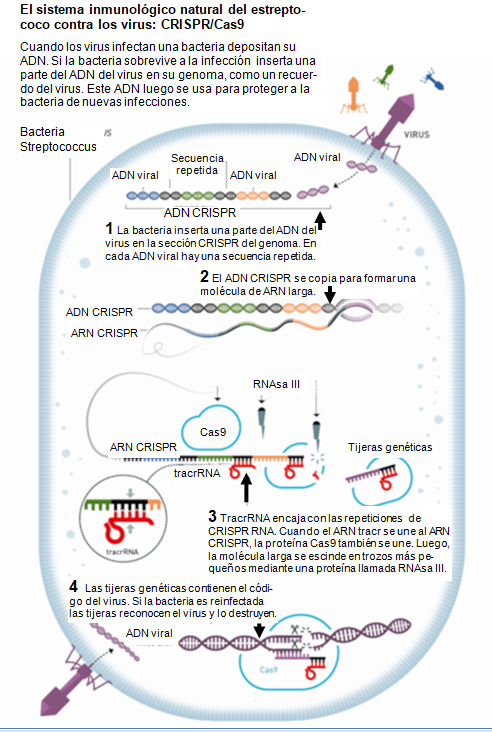
Figura 1 |
|
En la primavera de 2011,
después de conocerse en un congreso en Puerto Rico,
Carpentier y Doudna comienzan a colaborar. La sospecha
es que el CRISPR-ARN es necesario para identificar el
ADN de un virus y que Cas9 es la tijera que corta la
molécula de ADN.
Después de muchas
discusiones y numerosos experimentos fallidos añaden
ARN tracr a sus pruebas. Se creía que el
ARN tracr solo era necesario cuando CRISPR-ARN se
escindía en su forma activa (figura 2), pero una vez
que Cas9 tuvo acceso a ARN tracr, sucedió lo
que todos esperaban: la molécula de ADN se dividió en
dos partes.
La historia de las
tijeras genéticas podría haberse detenido aquí;
Charpentier y Doudna habían descubierto, en una
bacteria que causa un gran sufrimiento a la humanidad,
un mecanismo fundamental. Ese descubrimiento fue
asombroso en sí mismo, pero el azar favorece a las
mentes preparadas.
Los investigadores
deciden intentar simplificar las tijeras genéticas.
Usando lo que conocen sobre ARN tracr y CRISPR-ARN,
descubrieron cómo fusionar los dos en una sola
molécula, a la que llamaron ARN guía.
Con esta variante simplificada de las tijeras
genéticas emprenden un experimento que hace época,
investigan si pueden controlar esta herramienta
genética para que corte el ADN en un lugar previamente
seleccionado.
Saben que están cerca de
un gran avance. Toman un gen en el laboratorio de
Doudna y seleccionan cinco lugares diferentes donde el
gen debe dividirse. Luego cambian la parte CRISPR de
las tijeras para que su código coincida con el código
donde se realizarán los cortes (figura 2). El
resultado fue extraordinario. Las moléculas de ADN se
escindieron exactamente en los lugares seleccionados.
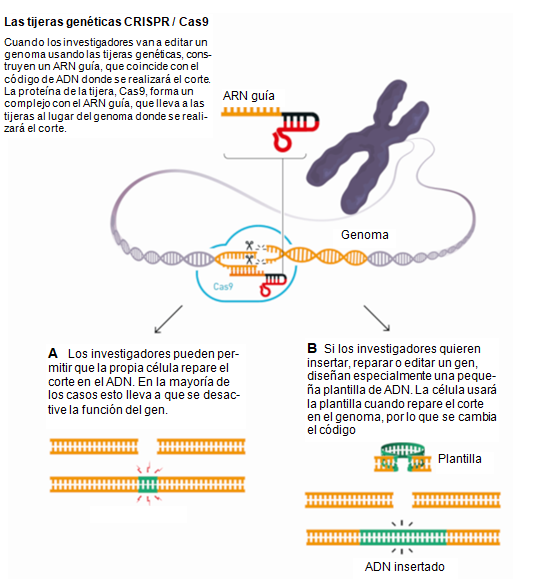
Figura 2 |
|
Poco después de que
Emmanuelle Charpentier y Jennifer Doudna publicaran su
descubrimiento de las tijeras genéticas CRISPR-Cas9 en
2012, varios grupos de investigación demuestran que
esta herramienta se puede utilizar para modificar el
genoma de las células, tanto de ratones como de
humanos, lo que lleva a un desarrollo explosivo. Hasta
la fecha cambiar los genes de una célula, planta u
organismo requería mucho tiempo y, a veces, era
imposible. Usando las tijeras genéticas los
investigadores pueden, en principio, hacer los cortes
que deseen en el genoma. Después de esto es fácil
utilizar los sistemas naturales de la célula para la
reparación del ADN de manera que reescriban el código
de la vida (figura 2).
Debido a que esta
herramienta genética es tan fácil de usar, actualmente
está muy extendida en la investigación básica. Se
utiliza para cambiar el ADN de células y animales de
laboratorio con el fin de comprender cómo funcionan e
interactúan los diferentes genes, por ejemplo, durante
el curso de una enfermedad.
Las tijeras genéticas
también se han convertido en una herramienta estándar
en el mejoramiento de los cultivos. Los métodos
utilizados anteriormente por los investigadores para
modificar los genomas de las plantas a menudo
requerían la adición de genes que podían producir
resistencia a los antibióticos. Cuando se realizan los
cultivos existe el riesgo de que esta resistencia a
los antibióticos se extienda a los microorganismos
circundantes. Gracias a las tijeras genéticas los
investigadores ya no necesitan utilizar estos métodos,
ya que ahora pueden realizar cambios muy precisos en
el genoma. Entre otras cosas han editado los genes que
hacen que el arroz absorba metales pesados del suelo,
lo que lleva a variedades mejoradas de arroz con
niveles más bajos de cadmio y arsénico. Los
investigadores también han desarrollado cultivos que
resisten mejor la sequía en un clima más cálido y que
resisten insectos y plagas que de otro modo tendrían
que ser combatidos con pesticidas.
En medicina las tijeras
genéticas están contribuyendo a desarrollar
inmunoterapias nuevas para el cáncer y se están
realizando ensayos para hacer realidad un sueño: curar
enfermedades hereditarias.
A pesar de los
beneficios que comportan, las tijeras genéticas
también pueden ser mal utilizadas. Se pueden usar, por
ejemplo, para crear embriones modificados
genéticamente. Sin embargo, durante muchos años, ha
habido leyes y regulaciones que controlan la
aplicación de la ingeniería genética, que incluyen
prohibiciones de modificar el genoma humano de una
manera que permita heredar los cambios. Además, los
experimentos que involucran a humanos y animales
siempre deben ser revisados y aprobados por comités de
ética antes de que se lleven a cabo.
Una cosa es cierta: esta
tecnología nos afectan a todos. Enfrentaremos nuevos
problemas éticos, pero esta nueva herramienta bien
puede contribuir a resolver muchos de los desafíos que
ahora enfrenta la humanidad. A través de su
descubrimiento, Emmanuelle Charpentier y
Jennifer Doudna desarrollaron una herramienta
que ha llevado las ciencias de la vida a una nueva
época. Nos han hecho contemplar un vasto horizonte de
potencial inimaginable y, en el camino, mientras
exploramos este nuevo territorio, tenemos la garantía
de realizar descubrimientos nuevos e inesperados.
|
|
|