|
Los sensores
situados en la superficie celular se denominan receptores.
Robert J. Lefkowitz y Brian K. Kobilka
han sido premiados con el Premio Nobel de Química
2012 por describir cómo funcionan una familia de
receptores llamados receptores acoplados a la G-proteína
(GPCRs). En esta familia encontramos receptores de la
adrenalina (también conocida como epinefrina), dopamina,
serotonina, luz, sabor y olor. La mayoría de los procesos
fisiológicos depende de los GPCRs. Aproximadamente la
mitad de todos los medicamentos actúan a través de estos
receptores, entre ellos están los beta bloqueantes,
antihistamínicos y varios tipos de fármacos psiquiátricos.
|
Los receptores
permanecieron sin identificar durante décadas. A pesar de
ello los científicos lograron desarrollar fármacos que
actuaban específicamente través de estos receptores. En la
década de 1940 el científico estadounidense Raymond Ahlquist, investigó cómo los diferentes órganos reaccionan
a diversas sustancias similares a la adrenalina. Su
trabajo lo llevó a concluir que debe haber dos tipos de
receptores para la adrenalina: uno que, fundamentalmente,
provoca la contracción de los vasos sanguíneos de las células
lisas de los músculos y otra que estimula principalmente
el corazón. Los llamó receptores alfa y beta. Poco después
se desarrollaron los primeros beta bloqueantes que actualmente son unos de los medicamentos
más utilizados en afecciones cardíacas.
Estas drogas sin duda alguna tenían efectos sobre las
células, pero cómo lo hacían seguía siendo un misterio.
Ahora sabemos por qué los receptores fueron tan difíciles
de encontrar: son relativamente escasos en número y
también en su mayoría están encapsulados dentro de la
pared de la célula. Después de un par de décadas, incluso Ahlquist comenzó a sentirse perdido con su teoría sobre los
dos tipos de receptores.
Y en este
punto, a finales de la década de 1960, Robert Lefkowitz,
uno de los galardonados este año con el Premio Nobel,
entra en la historia de los receptores.
Lefkowitz empieza a trabajar
con la hormona adrenocorticotropa (ACTH), que estimula la
producción de adrenalina en la glándula suprarrenal.
|
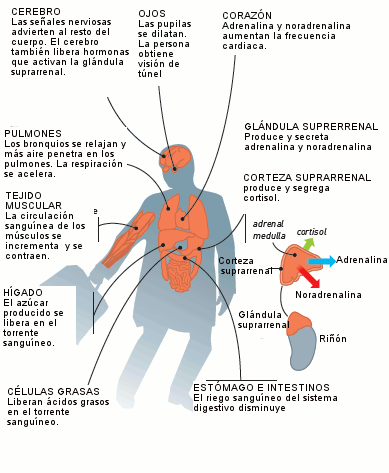
Reacción ante una
situación de peligro potencial. Las células de todo el
cuerpo sienten que algo está sucediendo gracias a sus
receptores
|
En 1970 publica artículos en dos
revistas prestigiosas, Proceedings of the National
Academy of Sciences (PNAS) and Science, donde
describe el descubrimiento de un receptor activo. El logro
le hace apreciar la emoción de hacer investigación y
recibe una oferta de la Universidad de Duke en Carolina
del Norte.
Trasladado a la
Universidad de Duke
en Carolina del Norte Lefkowitz forma su propio equipo de
investigación. Aunque parece que nunca se convertirá en un
cardiólogo(su plan inicial) quiere investigar sobre las
enfermedades del corazón. Así comienza centrándose en los
receptores de la adrenalina y noradrenalina, llamados
receptores adrenérgicos. Usando sustancias marcadas
radiactivamente, incluidos los bloqueadores beta, su grupo
de investigación estudia cómo trabajan estos receptores.
Después, depurando sus métodos, se las ingenian para
extraer una serie de receptores de los tejidos
En la década
de 1980, Lefkowitz decide que su grupo de investigación
debe intentar encontrar el gen que codifica el receptor
beta. Esta decisión sería crucial para la obtención del
Premio Nobel. Un gen es similar a un plano. Contiene un
código que es leído por la célula para unir los
aminoácidos que forman una proteína, por ejemplo, un
receptor. La idea era que si el grupo de investigación
pudiera leer las instrucciones para construir el receptor
beta, podrían obtener pistas sobre cómo funciona.
En esa época Lefkowitz contrata a un joven médico,
Brian Kobilka. La fascinación de Kobilka por los receptores
adrenérgicos nació de su experiencia hospitalaria en
terapia intensiva.
Kobilka se dedica a la caza de los genes. Una idea
ingeniosa le posibilita aislar el gen. Con gran
expectación los investigadores comienzan a analizar el
código; el análisis revela que el receptor se compone de
siete largas cadenas grasas (hidrofóbicas) en forma de
espiral llamadas hélices. Esto indica a los
científicos que el receptor probablemente se enrolle
siete veces, una y otra vez, a través de la pared
celular La rodopsina,
un receptor de luz que se encuentra en la retina, tiene
una estructura similar. Se sabía que los receptores adrenérgicos y la rodopsina
interactúan con proteínas G en el interior de la célula. Conclusión:
¡existe una familia de receptores similares y que
funcionan de la misma manera!
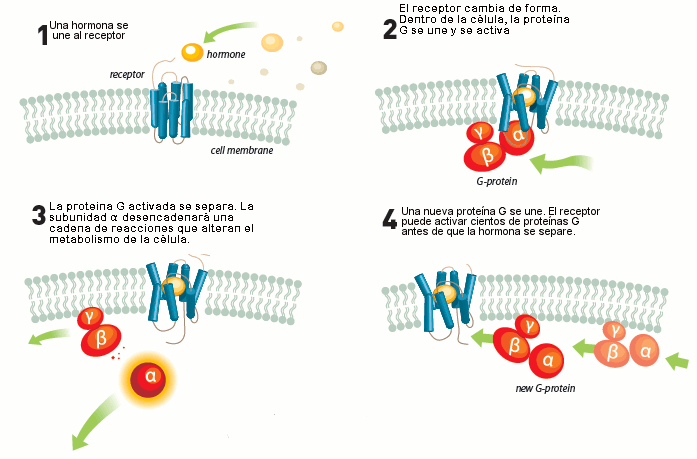
Cuando una
hormona, una molécula olfativa o del gusto, se enlaza con
un receptor en la superficie celular, se activa una cadena
de reacciones dentro de la célula.
Después del
éxito obtenido con el aislamiento del gen, Brian Kobilka se
trasladó a la Stanford University School of Medicine en
California. Allí comenzó a trabajar para crear una imagen
del receptor (un objetivo inalcanzable en la opinión de la
mayoría de la comunidad científica) un empeño que se
convertiría en un largo viaje.
Obtener la
imagen de una proteína es un proceso que implica muchos y
complicados pasos. Las proteínas son demasiado pequeñas
para ser vistas con los microscopios convencionales. Por
lo tanto, los científicos utilizan un método llamado
cristalografía de rayos x. Para empezar se debe de obtener
un cristal, en el cual las proteínas están cuidadosamente
embaladas en un patrón simétrico, como las moléculas de
agua en un cristal de hielo o los átomo de carbono en un
diamante. Después se hacen incidir rayos x sobre el
cristal de proteína. Cuando los rayos encuentran las
proteínas, son dispersados. Analizando el patrón de
difracción se puede deducir el aspecto de
las proteínas a nivel atómico
En la década
de 1950 se obtuvo la primera imagen de la estructura
cristalina de una proteína. Desde entonces se han radiografiado y fotografiado miles de proteínas. Sin
embargo la mayoría de ellas eran solubles en agua, lo que
facilita el proceso de cristalización. Muy pocos
investigadores habían obtenido imágenes de las proteínas
situadas en la membrana grasa de la célula. En agua tales
proteínas se disuelven muy mal formando pequeñas gotas,
como el aceite. Además, los GPCRs son por naturaleza muy
móviles (transmiten las señales moviéndose), pero dentro
de un cristal tienen que permanecer prácticamente quietos.
Conseguir cristales, por tanto, es un desafío
considerable.
Kobilka empleó
más de dos décadas para encontrar una solución a todos
estos problemas. Pero reuniendo determinación, creatividad
y biología molecular, Kobilka y su grupo de investigación
finalmente lograron su objetivo en 2011: consiguieron una
imagen del receptor en el mismo momento que transfiere la
señal desde la hormona en el exterior de la célula a la
proteína G en el interior
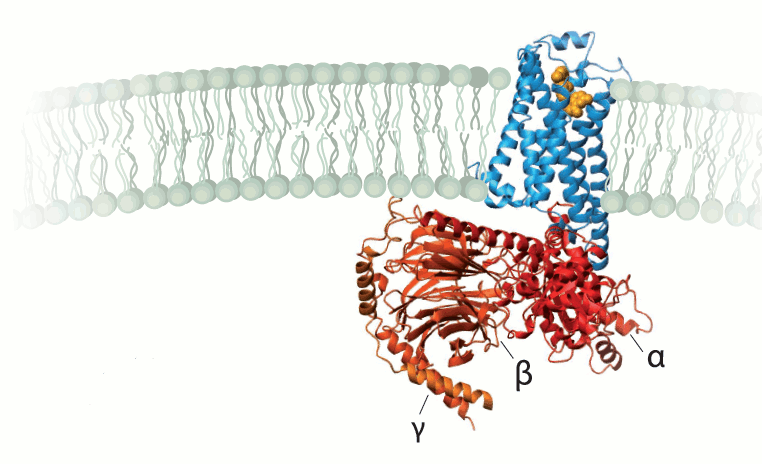
Ilustración
de la estructura de un cristal de Kobilka de un receptor
β-adrenérgico activado (azul). Puede verse una hormona (esferas
color naranja situadas en la parte superior de la imagen),
situada en el exterior de la célula y una proteína G (rojo),
unida al receptor, en
el interior.
|