|
El
agua no es absorbida o liberada por igual en todas las células o
tejidos. Desde mediados del s. XIX se ha sospechado que el flujo de
agua en determinados tejidos se realiza a través de proteínas con
poros que actúan como canales selectivos de agua.
En
1988 miembros del grupo de Agree descubrieron que la acuaporina
podía ser el tan buscado canal de agua.
Más
recientemente, en el año 2000, Agree publicó la primera estructura
tridimensional de la acuaporina.
Por
la acuaporina solo pasa agua neutra, H2O, pero no agua
protonada H3O+. Si no fuera así, el pH de la
célula cambiaría sin control. Para impedir el paso de agua
protonada o de otros cationes, el canal de la acuaporina posee
cargas positivas en su parte central que repelen a la carga
positiva del H3O+ impidiendo su entrada.
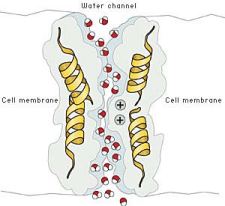
Hoy
se conocen unas 200 acuaporinas distintas pertenecientes a tejidos
de mamíferos, invertebrados, microorganismos y plantas |
Los
canales iónicos regulan, entre otras, las funciones del sistema
nervioso y de los músculos. En el impulso nervioso, un canal
iónico se abre en la superficie de una neurona como respuesta a una
señal química emitida por otra neurona vecina, y el pulso
eléctrico así generado se propaga mediante la apertura y cierre de
otros canales hasta la neurona siguiente, y todo ello en pocos
milisegundos.
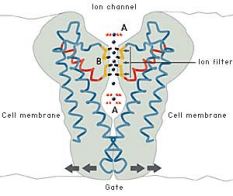
Siempre
ha resultado intrigante la selectividad de los canales de iones.
Tanto el Na+ como el K+, son cationes
esféricos co carga de 1,90 y 2,60 ángstroms, respectivamente.
¿Cómo explicar la selectividad del canal de potasio que no deja
pasar al sodio, un ión más pequeño?.
MacKinnon
explicaba en un artículo aparecido en Science (1 de abril de 1988)
el por qué de esta selectividad:
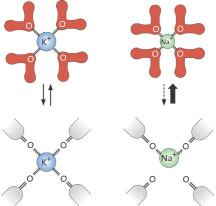
En
solución los iones están estabilizados por moléculas de agua que
los rodean (esfera de hidratación) . En el interior del canal, una
serie de átomos de oxígeno de la proteína se encuentran colocados
exactamente igual que los del agua alrededor del potasio antes de
entrar en el tubo, por lo que despojarse de su capa de hidratación
no le supone al potasio gasto alguno en energía. POr el contrario,
el sodio, al perder las moléculas de agua que lo estabilizan,
quedarían dentro del canal en una situación desfavorable, con los
oxígenos demasiado alejados. Podríamos afirmar que
"bailaría" dentro del tubo sin ajustarse perfectamente al
mismo, razón por la cual le resulta más rentable quedarse fuera.
|